Sommaire
1\ Phases, Systèmes.
Un minéral cristallin est un solide homogène et constitue en chimie physique une phase. Une roche est une association de minéraux (donc, une association de phases) et forme donc un Système.
Quand un système comporte plusieurs phases on le dit : hétérogène.
Un système peut subir des transformations internes ou bien, présenter des échanges avec l'extérieur. Un système est défini par son état qui est déterminé par des valeurs appelées « paramètres d'état ».
Un système est isolé quand il n'échange ni énergie ni matière avec l'extérieur.
Un système est fermé quand il échange de l'énergie avec l'extérieur mais qu'il n'échange pas de matière.
Un système est ouvert quand il échange de l'énergie et de la matière avec l'extérieur.
Restez informé !
Recevez nos derniers articles de géologie directement dans votre boîte mail.
Nous respectons votre vie privée. Désabonnement à tout moment.
Quand au cours de la transformation, la composition chimique ne varie pas (système fermé), on parle de transformation isochimique (-> topochimique).
Quand la composition chimique évolue, le système varie durant les transformations. Ces transformations sont dites allochimiques (= métasomatiques).
Le système peut associer plusieurs phases. Par exemple, dans le granit, on trouve trois phases : le quartz, le feldspath et le mica. L'eau pourrait être considérée comme une quatrième phase de ce système. C'est un système hétérogène. Si on fondait ce granit, le liquide obtenu serait un système homogène.
2\ Notion de constituants indépendants.
Les phases sont constituées d'éléments chimiques qui sont des constituants élémentaires. Les constituants indépendants sont des groupements chimiques nécessaires pour représenter toutes les phases.
Dans la wollastonite, SiO2 et CaO sont des constituants indépendants.
3\ Variable thermodynamique.
L'état est défini par des paramètres de deux types :
Intensifs, variable d'action : on y retrouve, la pression, la température, le potentiel chimique (µ) et les forces comme par exemple g-> (vecteur g) (gravité).
Extensifs, variables de position : S, G et H qui mesurent les modifications produites.
4\ Équilibre thermodynamique.
Un système est en équilibre quand il n'y a plus de transformation. Les variables de position qui définissent le système sont fixes. Si des transformations naturelles interviennent, on atteindra un nouvel état d'équilibre.
Dans un système à l'équilibre, il n'y a pas d'échange d'énergie dans, ou, entre les phases : aucune transformation spontanée n'est possible. On dit que le système est stable.
Si les possibilités de transformation persistent alors, on parle de système métastable.
5\ Règles de phase.
L'état est défini par des paramètres. La définition dépend de la température et de la pression de chacune des phases et du potentiel chimique de chacun des constituants.
Le nombre total de variables indépendantes dans un système simple à l'équilibre est égal au nombre de constituants indépendants + 2 (quelque soit le nombre de phases) : V = c + 2 – φ.
V est la variance, le nombre maximal de variables d'action que l'on peut choisir.
Cette règle exprime une relation entre le nombre de phases (pour nous, le nombre d'espèces minérales), le nombre de constituants et les variables pour les roches à l'équilibre.
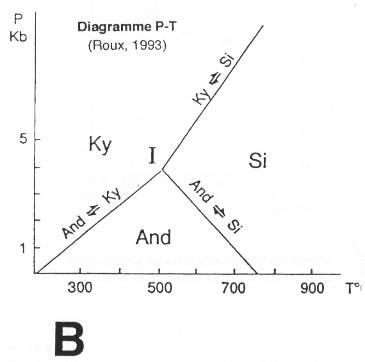
Il y a trois formes polymorphes de SiAl2O5.
- L'andalousite : BT, BP (Basse Température, Basse Pression).
- La sillimanite : HT.
- La kyanite (disthène) : HP.
L'andalousite et la sillimanite sont orthorhombiques. Le disthène est triclinique (plus dense).
Pour le domaine de l'andalousite, v = 1+ 2 – 1 = 2 → Il y a deux variables.
Sur la courbe de transformation (andalousite ↔ kyanite) : v = 1+2-2 = 1 → Il n'y a qu'une variable.
Le point I : c'est le point où l'on retrouve les 3 phases (v = 1+2-3 = 0).